Keemiline valem h2. Ainete keemilised nimetused ja valemid
Kovalentsete sidemete valemid erinevad põhimõtteliselt ioonsidemete valemitest. Fakt on see, et kovalentseid ühendeid saab moodustada mitmel viisil, mistõttu võivad reaktsiooni tulemusena tekkida erinevad ühendid.
1. Empiiriline valem
Empiiriline valem määrab molekuli moodustavad elemendid nende väikseimate täisarvude suhetes.
Näiteks C 2 H 6 O – ühend sisaldab kahte süsinikuaatomit, kuut vesinikuaatomit ja ühte hapnikuaatomit.
2. Molekulaarvalem
Molekulaarvalem näitab, millistest aatomitest ühend koosneb ja millistes kogustes neid aatomeid selles on.
Näiteks ühendi C2H6O molekulvalemid võivad olla järgmised: C4H12O2; C6H18O3...
Kovalentse ühendi täielikuks kirjeldamiseks ei piisa molekulaarvalemist:
Nagu näete, on mõlemal ühendil sama molekulvalem - C 2 H 6 O, kuid need on täiesti erinevad ained:
- dimetüüleetrit kasutatakse külmutusseadmetes;
- etüülalkohol on alkohoolsete jookide aluseks.
3. Struktuurivalem
Struktuurivalem on mõeldud kovalentse ühendi täpseks määramiseks, kuna lisaks ühendis sisalduvatele elementidele ja aatomite arvule näitab see ka ühendusskeemühendused.
Kasutatakse struktuurivalemit elektron-punkt valem Ja Lewise valem.
4. Vee (H 2 O) struktuurivalem
Vaatleme veemolekuli näitel struktuurivalemi koostamise protseduuri.
I Ühendusraami ehitamine
Ühendi aatomid on paigutatud ümber keskse aatomi. Kesksed aatomid on tavaliselt: süsinik, räni, lämmastik, fosfor, hapnik, väävel.

II Leia ühendi kõigi aatomite valentselektronide summa
Vee jaoks: H 2 O = (2 1 + 6) = 8
Vesinikuaatomil on üks valentselektron ja hapnikuaatomil 6. Kuna ühendis on kaks vesinikuaatomit, on valentselektronide koguarv veemolekulis 8.
III Määrata kovalentsete sidemete arv veemolekulis
Määratakse valemiga: S = N - A, Kus
S- molekulis jagatud elektronide arv;
N- valentselektronide summa, mis vastab ühendis olevate aatomite täielikule välisenergia tasemele:
N=2- vesinikuaatomi jaoks;
N = 8- teiste elementide aatomite jaoks
A- ühendi kõigi aatomite valentselektronide summa.
N = 2 2 + 8 = 12
A = 2 1 + 6 = 8
S = 12-8 = 4
Veemolekulis on jagatud elektrone 4. Kuna kovalentne side koosneb elektronide paarist, saame kaks kovalentset sidet.
IV Jagatud elektronide jaotamine
Keskse aatomi ja seda ümbritsevate aatomite vahel peab olema vähemalt üks side. Veemolekuli puhul on iga vesinikuaatomi jaoks kaks sellist sidet:

V Jaotage ülejäänud elektronid laiali
Kaheksast valentselektronist on neli juba jaotatud. Kuhu "panna" ülejäänud neli elektroni?
Igas ühendi aatomis peab olema täis oktett elektrone. Vesiniku puhul on see kaks elektroni; hapniku jaoks - 8.

Jagatud elektrone nimetatakse ühendamine.

Elektronpunkti valem ja Lewise valem kirjeldavad selgelt kovalentse sideme struktuuri, kuid on tülikad ja võtavad palju ruumi. Neid puudusi saab kasutades ära hoida kondenseeritud struktuurivalem, mis näitab ainult ühenduste järjekorda.
Lühendatud struktuurvalemi näide:
- dimetüüleeter - CH3OCH3
- etüülalkohol - C 2 H 5 OH
Keemiline valem on sümboleid kasutav pilt.
Keemiliste elementide märgid
Keemiline märk või keemilise elemendi sümbol– see on selle elemendi ladinakeelse nimetuse esimene või kaks esimest tähte.
Näiteks: FerrumFe , Cuprum -Cu , OxygeniumO jne.
Tabel 1: Keemilise märgiga antud teave
| Intelligentsus | Kasutades Cl näidet |
| Asja nimi | Kloor |
| Mittemetall, halogeen | |
| Üks element | 1 klooriaatom |
| (Ar) sellest elemendist | Ar(Cl) = 35,5 |
| Keemilise elemendi absoluutne aatommass
m = Ar 1,66 10 -24 g = Ar 1,66 10 -27 kg |
M (Cl) = 35,5 1,66 10 -24 = 58,9 10 -24 g |
Keemilise sümboli nimetus loetakse enamikul juhtudel keemilise elemendi nimeks. Näiteks, K – kaalium, Ca – kaltsium, Mg - magneesium, Mn – mangaan.
Juhud, mil keemilise sümboli nime loetakse erinevalt, on toodud tabelis 2:
| Keemilise elemendi nimi | Keemiline märk | Keemilise sümboli nimi
(hääldus) |
| Lämmastik | N | En |
| Vesinik | H | Tuhk |
| Raud | Fe | Ferrum |
| Kuldne | Au | Aurum |
| Hapnik | O | KOHTA |
| Räni | Si | Räni |
| Vask | Cu | Cuprum |
| Tina | Sn | Stanum |
| elavhõbe | Hg | Hüdrargium |
| Plii | Pb | Plumbum |
| Väävel | S | Es |
| Hõbedane | Ag | Argentum |
| Süsinik | C | Tse |
| Fosfor | P | Pe |
Lihtainete keemilised valemid
Enamike lihtsate ainete (kõik metallid ja paljud mittemetallid) keemilised valemid on vastavate keemiliste elementide märgid.
Niisiis raua aine Ja keemiline element raud on tähistatud samaks - Fe .
Kui sellel on molekulaarstruktuur (on olemas kujul , siis selle valem on elemendi keemiline märk indeks all paremal, mis näitab aatomite arv molekulis: H 2, O2, O 3, N 2, F 2, Cl2, BR 2, P 4, S 8.
Tabel 3: Keemilise märgiga antud teave
| Intelligentsus | Kasutades C näitena |
| Aine nimetus | Süsinik (teemant, grafiit, grafeen, karbüün) |
| Elemendi kuulumine antud keemiliste elementide klassi | Mittemetallist |
| Üks elemendi aatom | 1 süsinikuaatom |
| Suhteline aatommass (Ar) element, mis moodustab aine | Ar(C) = 12 |
| Absoluutne aatommass | M(C) = 12 1,66 10-24 = 19,93 10 -24 g |
| Üks aine | 1 mool süsinikku, s.o. 6.02 10 23 süsiniku aatomid |
| M (C) = Ar (C) = 12 g/mol |
Komplekssete ainete keemilised valemid
Keerulise aine valem koostatakse aine koosnevate keemiliste elementide märkide üleskirjutamisega, näidates iga elemendi aatomite arvu molekulis. Sel juhul kirjutatakse reeglina keemilised elemendid elektronegatiivsuse suurendamise järjekorras vastavalt järgmistele praktilistele seeriatele:
Mina, Si, B, Te, H, P, As, I, Se, C, S, Br, Cl, N, O, F
Näiteks, H2O , CaSO4 , Al2O3 , CS 2 , 2-st , NaH.
Erandid on järgmised:
- mõned lämmastikuühendid vesinikuga (näiteks ammoniaak NH3 , hüdrasiin N 2H 4 );
- orgaaniliste hapete soolad (näiteks naatriumformiaat HCOONa , kaltsiumatsetaat (CH 3COO) 2Ca) ;
- süsivesinikud ( CH 4 , C2H4 , C2H2 ).
Vormis esinevate ainete keemilised valemid dimeerid (EI 2 , P2O 3 , P2O5, monovalentse elavhõbeda soolad, näiteks: HgCl , HgNO3 jne), mis on kirjutatud kujul N 2 O4,P 4 O6,P 4 O 10Hg 2 Cl2,Hg 2 ( EI 3) 2 .
Mõiste alusel määratakse keemilise elemendi aatomite arv molekulis ja kompleksioonis valents või oksüdatsiooniseisundid ja salvestatakse indeks all paremal iga elemendi märgist (indeks 1 jäetakse välja). Sel juhul lähtuvad nad reeglist:
molekuli kõigi aatomite oksüdatsiooniastmete algebraline summa peab olema võrdne nulliga (molekulid on elektriliselt neutraalsed) ja kompleksioonis - iooni laeng.
Näiteks:
2Al 3 + +3SO 4 2- =Al 2 (SO 4) 3
Kasutatakse sama reeglit keemilise elemendi oksüdatsiooniastme määramisel aine või kompleksi valemi abil. Tavaliselt on see element, millel on mitu oksüdatsiooniastet. Ülejäänud molekuli või iooni moodustavate elementide oksüdatsiooniastmed peavad olema teada.
Kompleksse iooni laeng on kõigi iooni moodustavate aatomite oksüdatsiooniastmete algebraline summa. Seetõttu asetatakse kompleksioonis keemilise elemendi oksüdatsiooniastme määramisel ioon ise sulgudesse ja selle laeng võetakse sulgudest välja.
Valentsi valemite koostamisel ainet kujutatakse kahest erinevat tüüpi osakesest koosneva ühendina, mille valentsid on teada. Järgmisena kasutavad nad reegel:
molekulis peab valentsi korrutis ühte tüüpi osakeste arvu järgi olema võrdne valentsi korrutisega teist tüüpi osakeste arvuga.
Näiteks:
Nimetatakse arvu enne valemit reaktsioonivõrrandis koefitsient. Ta näitab kumbagi molekulide arv, või aine moolide arv.
Koefitsient enne keemilist sümbolit, näitab antud keemilise elemendi aatomite arv, ja juhul, kui märk on lihtaine valem, näitab koefitsient kumbagi aatomite arv, või selle aine moolide arv.
Näiteks:
- 3 Fe– kolm rauaaatomit, 3 mooli rauaaatomit,
- 2 H– kaks vesinikuaatomit, 2 mooli vesinikuaatomit,
- H 2– üks vesiniku molekul, 1 mool vesinikku.
Paljude ainete keemilised valemid on katseliselt määratud, mistõttu neid nimetatakse "empiiriline".
Tabel 4: Kompleksaine keemilise valemiga esitatud teave
| Intelligentsus | Näiteks C aCO3 |
| Aine nimetus | Kaltsiumkarbonaat |
| Elemendi kuulumine teatud ainete klassi | Keskmine (tavaline) sool |
| Üks aine molekul | 1 molekul kaltsiumkarbonaat |
| Üks mool ainet | 6.02 10 23 molekulid CaCO3 |
| Aine suhteline molekulmass (Mr) | Мr (CaCO3) = Ar (Ca) + Ar (C) + 3Ar (O) = 100 |
| Aine molaarmass (M) | M (CaCO3) = 100 g/mol |
| Aine absoluutne molekulmass (m) | M (CaCO3) = Mr (CaCO3) 1,66 10 -24 g = 1,66 10 -22 g |
| Kvalitatiivne koostis (millised keemilised elemendid moodustavad aine) | kaltsium, süsinik, hapnik |
| Aine kvantitatiivne koostis: | |
| Iga elemendi aatomite arv aine ühes molekulis: | kaltsiumkarbonaadi molekul koosneb 1 aatom kaltsium, 1 aatom süsinik ja 3 aatomit hapnikku. |
| Iga elemendi moolide arv 1 mooli aine kohta: | 1 moolis CaCO 3(6,02 · 10 23 molekuli) sisalduvad 1 mutt(6,02 · 10 23 aatomit) kaltsium, 1 mutt(6,02 10 23 aatomit) süsiniku ja 3 mol(3 6,02 10 23 aatomit) keemilise elemendi hapnik) |
| Aine massikoostis: | |
| Iga elemendi mass 1 mooli aine kohta: | 1 mool kaltsiumkarbonaati (100 g) sisaldab järgmisi keemilisi elemente: 40 g kaltsiumi, 12 g süsinikku, 48 g hapnikku. |
| Aine keemiliste elementide massiosad (aine koostis massiprotsentides):
|
Kaltsiumkarbonaadi koostis massi järgi:
W (Ca) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (1,40)/100 = 0,4 (40%) W (C) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (1 12) / 100 = 0,12 (12%) W (O) = (n (Ca) Ar (Ca))/Mr (CaCO3) = (3 16)/100 = 0,48 (48%) |
| Ioonse struktuuriga aine (sool, hape, alus) puhul annab aine valem teavet igat tüüpi ioonide arvu kohta molekulis, nende koguse ja ioonide massi kohta 1 mooli aine kohta:
|
Molekul CaCO 3 koosneb ioonist Ca 2+ ja ioon CO 3 2-
1 mol ( 6.02 10 23 molekulid) CaCO 3 sisaldab 1 mol Ca 2+ ioone Ja 1 mool ioone CO 3 2-; 1 mool (100 g) kaltsiumkarbonaati sisaldab 40 g ioone Ca 2+ Ja 60 g ioone CO 3 2- |
| Aine molaarmaht standardtingimustes (ainult gaaside puhul) | |
Graafilised valemid
Aine kohta täielikuma teabe saamiseks kasutage graafilised valemid , mis näitavad Aatomite ühendamise järjekord molekulis Ja iga elemendi valents.
Molekulidest koosnevate ainete graafilised valemid peegeldavad mõnikord ühel või teisel määral nende molekulide struktuuri (struktuuri), sel juhul võib neid nimetada. struktuurne .
Aine graafilise (struktuurse) valemi koostamiseks peate:
- Määrake kõigi ainet moodustavate keemiliste elementide valents.
- Kirjutage üles kõigi ainet moodustavate keemiliste elementide märgid, millest igaüks on võrdne antud elemendi aatomite arvuga molekulis.
- Ühendage keemiliste elementide märgid kriipsudega. Iga kriips tähistab paari, mis suhtleb keemiliste elementide vahel ja kuulub seetõttu võrdselt mõlema elemendi hulka.
- Keemilise elemendi märki ümbritsevate joonte arv peab vastama selle keemilise elemendi valentsile.
- Hapnikku sisaldavate hapete ja nende soolade valmistamisel seotakse vesiniku- ja metalliaatomid hapet moodustava elemendiga läbi hapnikuaatomi.
- Hapnikuaatomid kombineeritakse omavahel ainult peroksiidide valmistamisel.
Graafiliste valemite näited:
Anorgaaniliste ainete klassifikatsioon ja nende nomenklatuur põhinevad kõige lihtsamal ja ajas püsivamal tunnusel - keemiline koostis, mis näitab antud ainet moodustavate elementide aatomeid nende arvulises vahekorras. Kui aine koosneb ühe keemilise elemendi aatomitest, s.o. on selle elemendi olemasolu vorm vabas vormis, siis nimetatakse seda lihtsaks aine; kui aine koosneb kahe või enama elemendi aatomitest, siis seda nimetatakse kompleksne aine. Tavaliselt nimetatakse kõiki lihtaineid (v.a. monoatomilised) ja kõiki kompleksaineid keemilised ühendid, kuna neis on ühe või erinevate elementide aatomid omavahel ühendatud keemiliste sidemetega.
Anorgaaniliste ainete nomenklatuur koosneb valemitest ja nimetustest. Keemiline valem - aine koostise kujutamine keemiliste elementide sümbolite, arvindeksite ja mõningate muude märkide abil. Keemiline nimetus - pilt aine koostisest, kasutades sõna või sõnarühma. Keemiliste valemite ja nimetuste konstruktsiooni määrab süsteem nomenklatuuri reeglid.
Keemiliste elementide sümbolid ja nimetused on toodud elementide perioodilises tabelis D.I. Mendelejev. Elemendid on tavapäraselt jagatud metallid Ja mittemetallid . Mittemetallide hulka kuuluvad kõik VIIIA rühma (väärisgaasid) ja VIIA rühma (halogeenid) elemendid, VIA rühma elemendid (va poloonium), elemendid lämmastik, fosfor, arseen (VA rühm); süsinik, räni (IVA rühm); boor (IIIA rühm), samuti vesinik. Ülejäänud elemendid klassifitseeritakse metallideks.
Ainete nimetuste koostamisel kasutatakse tavaliselt elementide venekeelseid nimetusi, näiteks dihapnik, ksenoondifluoriid, kaaliumselenaat. Traditsiooniliselt lisatakse mõne elemendi ladinakeelsete nimede juured tuletisterminitesse:
Näiteks: karbonaat, manganaat, oksiid, sulfiid, silikaat.
Pealkirjad lihtsad ained koosnevad ühest sõnast - keemilise elemendi nimi numbrilise eesliitega, näiteks:
Kasutatakse järgmisi numbrilised eesliited:
Määramatu arv on tähistatud numbrilise eesliitega n- polü.
Mõne lihtsa aine puhul kasutavad nad ka eriline nimetused nagu O 3 - osoon, P 4 - valge fosfor.
Keemilised valemid komplekssed ained koosneb nimetusest elektropositiivne(tinglikud ja tegelikud katioonid) ja elektronegatiivne(tingimuslikud ja reaalsed anioonid) komponendid, näiteks CuSO 4 (siin Cu 2+ on reaalne katioon, SO 4 2 - reaalne anioon) ja PCl 3 (siin P +III on tingimuslik katioon, Cl -I on tingimuslik anioon).
Pealkirjad komplekssed ained koostatud keemiliste valemite järgi paremalt vasakule. Need koosnevad kahest sõnast - elektronegatiivsete komponentide nimed (nimetavas käändes) ja elektropositiivsed komponendid (genitiivses käändes), näiteks:
CuSO 4 - vask(II)sulfaat
PCl 3 - fosfortrikloriid
LaCl 3 - lantaan(III)kloriid
CO - süsinikmonooksiid
Elektropositiivsete ja elektronegatiivsete komponentide arv nimedes on näidatud ülaltoodud numbriliste eesliidetega (universaalne meetod) või oksüdatsiooniastmetega (kui neid saab valemiga määrata), kasutades sulgudes rooma numbreid (plussmärk jäetakse välja). Mõnel juhul on ioonide laeng antud (keerulise koostisega katioonide ja anioonide puhul), kasutades vastava märgiga araabia numbreid.
Levinud mitmeelemendiliste katioonide ja anioonide jaoks kasutatakse järgmisi erinimetusi:
|
H 2 F + - fluoroonium |
C 2 2 - - atsetüleniid |
|
H 3 O + - oksoonium |
CN - - tsüaniid |
|
H 3 S + - sulfoonium |
CNO - - fulminaat |
|
NH 4 + - ammoonium |
HF 2 - - vesinikdifluoriid |
|
N2H5+-hüdrasiinium(1+) |
HO 2 - - hüdroperoksiid |
|
N2H6+-hüdrasiinium(2+) |
HS - - vesiniksulfiid |
|
NH 3 OH + - hüdroksüülamiin |
N3 - - asiid |
|
NO+ - nitrosüül |
NCS - - tiotsüanaat |
|
NO 2 + - nitroüül |
O 2 2 - - peroksiid |
|
O 2 + - dioksügenüül |
O 2 - - superoksiid |
|
PH 4 + - fosfoonium |
O 3 - - osoniid |
|
VO 2+ - vanadüül |
OCN - - tsüanaat |
|
UO 2+ - uranüül |
OH - - hüdroksiid |
Seda kasutatakse ka vähese hulga tuntud ainete puhul eriline pealkirjad:
1. Happelised ja aluselised hüdroksiidid. soolad
Hüdroksiidid on teatud tüüpi kompleksained, mis sisaldavad mõne elemendi E aatomeid (va fluor ja hapnik) ja hüdroksüülrühmi OH; hüdroksiidide üldvalem E(OH) n, Kus n= 1÷6. Hüdroksiidide vorm E(OH) n helistas orto- kuju; juures n> 2 hüdroksiidi võib leida ka meta-vorm, mis sisaldab lisaks E-aatomitele ja OH-rühmadele ka hapnikuaatomeid O, näiteks E(OH)3 ja EO(OH), E(OH)4 ja E(OH)6 ning EO2(OH)2 .
Hüdroksiidid jagunevad kahte vastandlike keemiliste omadustega rühma: happelised ja aluselised hüdroksiidid.
Happelised hüdroksiidid sisaldavad vesinikuaatomeid, mida saab asendada metalliaatomitega, mille suhtes kehtivad stöhhiomeetrilise valentsi reeglid. Enamik happehüdroksiide leidub meta-vorm ja happeliste hüdroksiidide valemites on esikohal vesinikuaatomid, näiteks H 2 SO 4, HNO 3 ja H 2 CO 3, mitte SO 2 (OH) 2, NO 2 (OH) ja CO ( oh) 2. Happehüdroksiidide üldvalem on H X EO juures, kus elektronegatiivne komponent EO y x - nimetatakse happejäägiks. Kui kõiki vesinikuaatomeid ei asendata metalliga, jäävad nad happejäägi osaks.
Tavaliste happehüdroksiidide nimetused koosnevad kahest sõnast: pärisnimi lõpuga "aya" ja rühmasõna "hape". Siin on tavaliste happehüdroksiidide ja nende happeliste jääkide valemid ja pärisnimed (kriips tähendab, et hüdroksiid ei ole teada vabas vormis ega happelises vesilahuses):
|
happehüdroksiid |
happejääk |
|
HAsO 2 - metaarsenic |
AsO 2 - - metaarseniit |
|
H 3 AsO 3 - ortoarseen |
AsO 3 3 - - ortoarseniit |
|
H 3 AsO 4 - arseen |
AsO 4 3 - - arsenaat |
|
B 4 O 7 2 - - tetraboraat |
|
|
ВiО 3 - - vismutaat |
|
|
HBrO - bromiid |
BrO - - hüpobromiit |
|
HBrO 3 - broomitud |
BrO 3 - - bromaat |
|
H 2 CO 3 - kivisüsi |
CO 3 2 - - karbonaat |
|
HClO - hüpokloorne |
ClO- - hüpoklorit |
|
HClO 2 - kloriid |
ClO2 - - klorit |
|
HClO 3 - kloor |
ClO3 - - kloraat |
|
HClO 4 - kloor |
ClO4 - - perkloraat |
|
H 2 CrO 4 - kroom |
CrO 4 2 - - kromaat |
|
НCrO 4 - - hüdrokromaat |
|
|
H 2 Cr 2 O 7 - dikroomne |
Cr 2 O 7 2 - - dikromaat |
|
FeO42- - ferraat |
|
|
HIO 3 - jood |
IO 3 - - jodaat |
|
HIO 4 - metaiodiin |
IO 4 - - metaperiodaat |
|
H 5 IO 6 - ortojood |
IO 6 5 - - ortoperiodaat |
|
HMnO 4 - mangaan |
MnO4- - permanganaat |
|
MnO42- - manganaat |
|
|
MoO 4 2 - - molübdaat |
|
|
HNO 2 - lämmastik |
EI 2 - - nitrit |
|
HNO 3 - lämmastik |
NR 3 - - nitraat |
|
HPO 3 - metafosforne |
PO 3 - - metafosfaat |
|
H 3 PO 4 - ortofosfor |
PO 4 3 - - ortofosfaat |
|
НPO 4 2 - - hüdroortofosfaat |
|
|
H 2 PO 4 - - dihüdrootofosfaat |
|
|
H 4 P 2 O 7 - difosfor |
P 2 O 7 4 - - difosfaat |
|
ReO 4 - - perrhenaat |
|
|
SO 3 2 - - sulfit |
|
|
HSO 3 - - hüdrosulfit |
|
|
H 2 SO 4 - väävelhape |
SO 4 2 - - sulfaat |
|
HSO 4 - - vesiniksulfaat |
|
|
H 2S 2 O 7 - diväävel |
S 2 O 7 2 - - disulfaat |
|
H 2 S 2 O 6 (O 2) - peroksodiväävel |
S2O6 (O2)2- - peroksodisulfaat |
|
H 2 SO 3 S - tioväävel |
SO 3 S 2 - - tiosulfaat |
|
H 2 SeO 3 - seleen |
SeO 3 2 - - seleniit |
|
H 2 SeO 4 - seleen |
SeO 4 2 - - selenaat |
|
H 2 SiO 3 - metaräni |
SiO 3 2 - - metasilikaat |
|
H 4 SiO 4 - ortosilikoon |
SiO 4 4 - - ortosilikaat |
|
H 2 TeO 3 - telluur |
TeO 3 2 - - telluriit |
|
H 2 TeO 4 - metatelluurne |
TeO 4 2 - - metatellureerima |
|
H 6 TeO 6 - orthotelluric |
TeO 6 6 - - orthotellurate |
|
VO 3 - - metavanadaat |
|
|
VO 4 3 - - ortohovanadaat |
|
|
WO 4 3 - - volframaat |
Vähem levinud happehüdroksiidid nimetatakse vastavalt kompleksühendite nomenklatuurireeglitele, näiteks:
Happejääkide nimetusi kasutatakse soolade nimetuste koostamiseks.
Aluselised hüdroksiidid sisaldavad hüdroksiidiioone, mida saab stöhhiomeetrilise valentsi reegli kohaselt asendada happejääkidega. Kõik aluselised hüdroksiidid on leitud orto- kuju; nende üldvalem on M(OH) n, Kus n= 1,2 (harvemini 3,4) ja M n+ on metalli katioon. Aluseliste hüdroksiidide valemite ja nimetuste näited:
Aluseliste ja happeliste hüdroksiidide kõige olulisem keemiline omadus on nende vastastikmõju soolade moodustamiseks ( soola moodustumise reaktsioon), Näiteks:
Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
Ca(OH)2 + 2H2SO4 = Ca(HSO4)2 + 2H2O
2Ca(OH)2 + H2SO4 = Ca2SO4(OH)2 + 2H2O
Soolad on teatud tüüpi komplekssed ained, mis sisaldavad M katioone n+ ja happelised jäägid*.
Soolad üldvalemiga M X(EO juures)n helistas keskmine soolad ja soolad asendamata vesinikuaatomitega - hapu soolad. Mõnikord sisaldavad soolad ka hüdroksiidi ja/või oksiidiioone; selliseid sooli nimetatakse peamine soolad. Siin on soolade näited ja nimetused:
|
Kaltsiumortofosfaat |
|
|
Kaltsiumdivesinikortofosfaat |
|
|
Kaltsiumvesinikfosfaat |
|
|
Vask(II)karbonaat |
|
|
Cu 2 CO 3 (OH) 2 |
Divaskdihüdroksiidkarbonaat |
|
Lantaan(III)nitraat |
|
|
Titaanoksiiddinitraat |
Happeid ja aluselisi sooli saab muundada keskmisteks sooladeks, reageerides sobiva aluselise ja happelise hüdroksiidiga, näiteks:
Ca(HSO 4) 2 + Ca(OH) = CaSO 4 + 2H 2 O
Ca 2 SO 4 (OH) 2 + H 2 SO 4 = Ca 2 SO 4 + 2 H 2 O
On ka sooli, mis sisaldavad kahte erinevat katiooni: neid nimetatakse sageli topeltsoolad, Näiteks:
2. Happelised ja aluselised oksiidid
Oksiidid E X KOHTA juures- hüdroksiidide täieliku dehüdratsiooni saadused:
Happelised hüdroksiidid (H 2 SO 4, H 2 CO 3) happeoksiidid vastus(SO 3, CO 2) ja aluselised hüdroksiidid (NaOH, Ca(OH) 2) - põhilisedoksiidid(Na 2 O, CaO) ja elemendi E oksüdatsiooniaste ei muutu hüdroksiidilt oksiidiks üleminekul. Valemite ja oksiidide nimetuste näide:
Happelised ja aluselised oksiidid säilitavad vastandlike omadustega hüdroksiididega või omavahel suhtlemisel vastavate hüdroksiidide soola moodustavad omadused:
N 2 O 5 + 2 NaOH = 2 NaNO 3 + H 2 O
3CaO + 2H3PO4 = Ca3(PO4)2 + 3H2O
La 2 O 3 + 3SO 3 = La 2 (SO 4) 3
3. Amfoteersed oksiidid ja hüdroksiidid
Amfoteersus hüdroksiidid ja oksiidid - keemiline omadus, mis seisneb nende poolt kahe soolarea moodustamises, näiteks alumiiniumhüdroksiidi ja alumiiniumoksiidi jaoks:
(a) 2Al(OH)3 + 3SO3 = Al2(SO4)3 + 3H2O
Al 2 O 3 + 3 H 2 SO 4 = Al 2 ( SO 4 ) 3 + 3 H 2 O
(b) 2Al(OH)3 + Na2O = 2NaAlO2 + 3H2O
Al 2 O 3 + 2 NaOH = 2 NaAlO 2 + H 2 O
Seega on alumiiniumhüdroksiidil ja oksiidil reaktsioonides (a) omadused peamine hüdroksiidid ja oksiidid, s.o. reageerivad happeliste hüdroksiidide ja oksiidiga, moodustades vastava soola - alumiiniumsulfaadi Al 2 (SO 4) 3, samas kui reaktsioonides (b) on neil ka omadused happeline hüdroksiidid ja oksiidid, s.o. reageerivad aluselise hüdroksiidi ja oksiidiga, moodustades soola - naatriumdioksoaluminaat (III) NaAlO 2. Esimesel juhul on elemendil alumiinium metalli omadus ja see on osa elektropositiivsest komponendist (Al 3+), teisel juhul mittemetalli omadus ja on osa soola valemi elektronegatiivsest komponendist ( AlO2-).
Kui need reaktsioonid toimuvad vesilahuses, muutub saadud soolade koostis, kuid alumiiniumi olemasolu katioonis ja anioonis jääb alles:
2Al(OH)3 + 3H2SO4 = 2(SO4)3
Al(OH)3 + NaOH = Na
Siin on nurksulgudes esile tõstetud kompleksioonid 3+ - heksaakvaalumiinium(III) katioon, - - tetrahüdroksoaluminaat(III) ioon.
Elemente, millel on ühendites metallilised ja mittemetallilised omadused, nimetatakse amfoteersteks, nende hulka kuuluvad perioodilisuse tabeli A-rühmade elemendid - Be, Al, Ga, Ge, Sn, Pb, Sb, Bi, Po jne. nagu ka enamik B-rühmade elemente - Cr, Mn, Fe, Zn, Cd, Au jne. Amfoteersed oksiidid on samad, mis aluselised, näiteks:
Amfoteersed hüdroksiidid (kui elemendi oksüdatsiooniaste ületab + II) võib leida orto- või (ja) meta- vorm. Siin on näited amfoteersetest hüdroksiididest:
Amfoteersed oksiidid ei vasta alati amfoteersetele hüdroksiididele, kuna viimaste saamiseks tekivad hüdraatoksiidid, näiteks:
Kui amfoteersel elemendil ühendis on mitu oksüdatsiooniastet, siis vastavate oksiidide ja hüdroksiidide amfoteersus (ja sellest tulenevalt ka elemendi enda amfoteersus) väljendub erinevalt. Madala oksüdatsiooniastme korral on hüdroksiididel ja oksiididel ülekaalus põhiomadused ning elemendil endal on metallilised omadused, mistõttu see sisaldub peaaegu alati katioonide koostises. Vastupidi, kõrgete oksüdatsiooniastmete korral on hüdroksiididel ja oksiididel ülekaalus happelised omadused ning elemendil endal on mittemetallilised omadused, nii et see sisaldub peaaegu alati anioonide koostises. Seega on mangaan(II)oksiidil ja -hüdroksiidil domineerivad aluselised omadused ning mangaan ise on osa 2+ tüüpi katioonidest, samas kui mangaan(VII)oksiidil ja -hüdroksiidil on domineerivad happelised omadused ning mangaan ise on osa MnO 4-st. tüüpi anioon.. Amfoteersed hüdroksiidid, millel on suur happeliste omaduste ülekaal, omistatakse happeliste hüdroksiidide järgi modelleeritud valemid ja nimetused, näiteks HMn VII O 4 - mangaanhape.
Seega on elementide jaotus metallideks ja mittemetallideks tingimuslik; Puhtalt metalliliste omadustega elementide (Na, K, Ca, Ba jne) ja puhtalt mittemetalliliste omadustega elementide (F, O, N, Cl, S, C jne) vahel on suur rühm. amfoteersete omadustega elementidest.
4. Binaarsed ühendid
Laia tüüpi anorgaanilisi kompleksaineid on binaarsed ühendid. Nende hulka kuuluvad ennekõike kõik kaheelemendilised ühendid (v.a aluselised, happelised ja amfoteersed oksiidid), näiteks H 2 O, KBr, H 2 S, Cs 2 (S 2), N 2 O, NH 3, HN 3, CaC2, SiH4. Nende ühendite valemite elektropositiivsed ja elektronegatiivsed komponendid hõlmavad sama elemendi üksikuid aatomeid või seotud aatomite rühmi.
Mitmeelemendilisi aineid, mille valemis üks komponentidest sisaldab mitme elemendi mitteseotud aatomeid, samuti ühe- või mitmeelemendilisi aatomirühmi (va hüdroksiidid ja soolad), loetakse kahekomponentseteks ühenditeks, näiteks CSO, IO 2 F 3, SBrO 2 F, CrO (O 2) 2, PSI 3, (CaTi)O 3, (FeCu)S 2, Hg(CN) 2, (PF 3) 2 O, VCl 2 (NH 2). Seega võib CSO-d kujutada CS2 ühendina, milles üks väävliaatom on asendatud hapnikuaatomiga.
Binaarsete ühendite nimed konstrueeritakse tavaliste nomenklatuurireeglite järgi, näiteks:
|
OF 2 - hapniku difluoriid |
K 2 O 2 - kaaliumperoksiid |
|
HgCl 2 - elavhõbe(II)kloriid |
Na 2 S - naatriumsulfiid |
|
Hg 2 Cl 2 - dielavhõbedikloriid |
Mg 3 N 2 - magneesiumnitriid |
|
SBr 2 O - vääveloksiid-dibromiid |
NH 4 Br - ammooniumbromiid |
|
N 2 O - lämmastikoksiid |
Pb(N 3) 2 - plii(II)asiid |
|
NO 2 - lämmastikdioksiid |
CaC 2 - kaltsiumatsetüleniid |
Mõnede binaarsete ühendite puhul kasutatakse spetsiaalseid nimetusi, mille loetelu oli varem antud.
Binaarsete ühendite keemilised omadused on üsna mitmekesised, mistõttu jaotatakse need sageli anioonide nimetuste järgi rühmadesse, s.t. Eraldi vaadeldakse halogeniide, kalkogeniide, nitriide, karbiide, hüdriide jne Binaarsete ühendite hulgas on ka selliseid, millel on mõned muud tüüpi anorgaaniliste ainete omadused. Seega ei saa ühendeid CO, NO, NO 2 ja (Fe II Fe 2 III) O 4, mille nimetused on konstrueeritud kasutades sõna oksiid, liigitada oksiidideks (happelised, aluselised, amfoteersed). Süsinikmonooksiid CO, lämmastikmonooksiid NO ja lämmastikdioksiid NO 2 ei sisalda vastavaid happehüdroksiide (kuigi need oksiidid moodustavad mittemetallid C ja N), samuti ei moodusta nad sooli, mille anioonid sisaldaksid aatomeid C II, N II ja N IV. Topeltoksiid (Fe II Fe 2 III) O 4 - diraud(III)-raud(II)oksiid, kuigi sisaldab elektropositiivses komponendis amfoteerse elemendi - raua aatomeid, kuid kahes erinevas oksüdatsiooniastmes, mille tulemusena , interakteerudes happehüdroksiididega, moodustab see mitte ühe, vaid kaks erinevat soola.
Binaarsed ühendid nagu AgF, KBr, Na 2 S, Ba(HS) 2, NaCN, NH 4 Cl ja Pb(N 3) 2 koosnevad sarnaselt sooladega tõelistest katioonidest ja anioonidest, mistõttu neid nimetatakse. soolataoline binaarsed ühendid (või lihtsalt soolad). Neid võib pidada vesinikuaatomite asendusproduktideks ühendites HF, HCl, HBr, H2S, HCN ja HN3. Viimastel vesilahuses on happeline funktsioon ja seetõttu nimetatakse nende lahuseid hapeteks, näiteks HF (aqua) - vesinikfluoriidhape, H 2 S (aqua) - vesiniksulfiidhape. Kuid need ei kuulu happehüdroksiidide tüüpi ja nende derivaadid ei kuulu anorgaaniliste ainete klassifikatsiooni soolade hulka.
2.1. Keemiline keel ja selle osad
Inimkond kasutab palju erinevaid keeli. Välja arvatud loomulikud keeled(jaapani, inglise, vene - kokku üle 2,5 tuhande), on ka tehiskeeled, näiteks esperanto. Tehiskeelte hulgas on keeled mitmesugused teadused. Nii et keemias kasutavad nad oma, keemiline keel.
Keemiline keel– sümbolite ja mõistete süsteem, mis on loodud keemilise teabe lühikeseks, kokkuvõtlikuks ja visuaalseks salvestamiseks ja edastamiseks.
Enamikus loomulikes keeltes kirjutatud sõnum jaguneb lauseteks, laused sõnadeks ja sõnad tähtedeks. Kui nimetada lauseid, sõnu ja tähti keele osadeks, siis sarnaseid osi saame tuvastada ka keemilises keeles (tabel 2).
Tabel 2.Keemilise keele osad
Ühtegi keelt pole võimalik kohe omandada, see kehtib ka keemilise keele kohta. Seetõttu tutvute praegu ainult selle keele põhitõdedega: õppige "tähti", õppige mõistma "sõnade" ja "lausete" tähendust. Selle peatüki lõpus tutvustatakse teile nimed keemilised ained on keemilise keele lahutamatu osa. Keemiat õppides avarduvad ja süvenevad sinu teadmised keemiakeelest.
KEEMILINE KEEL.
1.Milliseid tehiskeeli oskate (peale õpiku tekstis mainitud)?
2. Mille poolest erinevad loomulikud keeled tehiskeeltest?
3. Kas arvate, et keemilisi nähtusi on võimalik kirjeldada ilma keemiakeelt kasutamata? Kui ei, siis miks mitte? Kui jah, siis millised oleksid sellise kirjelduse eelised ja puudused?
2.2. Keemiliste elementide sümbolid
Keemilise elemendi sümbol tähistab elementi ennast või selle elemendi ühte aatomit.
Iga selline sümbol on keemilise elemendi lühendatud ladinakeelne nimetus, mis koosneb ühest või kahest ladina tähestiku tähest (ladina tähestiku kohta vt 1. lisa). Sümbol kirjutatakse suure algustähega. Sümbolid ning mõne elemendi vene- ja ladinakeelsed nimetused on toodud tabelis 3. Seal on ka teave ladinakeelsete nimede päritolu kohta. Sümbolite hääldamisel pole üldreeglit, seetõttu on tabelis 3 toodud ka sümboli “lugemine” ehk kuidas seda sümbolit keemilises valemis loetakse.
Suulises kõnes ei saa elemendi nime asendada sümboliga, kuid käsitsi kirjutatud või trükitud tekstides on see lubatud, kuid mitte soovitatav.Praegu on teada 110 keemilist elementi, neist 109-l on Rahvusvaheliselt kinnitatud nimed ja sümbolid Puhta ja rakenduskeemia liit (IUPAC).
Tabel 3 sisaldab teavet ainult 33 elemendi kohta. Need on elemendid, millega keemiat õppides esimesena kokku puutute. Kõigi elementide venekeelsed nimetused (tähestikulises järjekorras) ja sümbolid on toodud lisas 2.
Tabel 3.Mõnede keemiliste elementide nimetused ja sümbolid
Nimi |
||||
ladina keel |
Kirjutamine |
|||
| - | Kirjutamine |
Päritolu |
- | - |
| Lämmastik | N itrogeenium | Kreeka keelest "salpeetri sünnitamine" | "en" | |
| Alumiiniumist | Al alumiinium | Alates Lat. "maarjas" | "alumiinium" | |
| Argoon | Ar gon | Kreeka keelest "mitteaktiivne" | "argoon" | |
| Baarium | Ba rium | Kreeka keelest "raske" | "baarium" | |
| Bor | B orum | Araabia keelest "valge mineraal" | "boor" | |
| Broom | Br omum | Kreeka keelest "haisev" | "broomi" | |
| Vesinik | H vesinik | Kreeka keelest "vee sünnitamine" | "tuhk" | |
| Heelium | Ta lium | Kreeka keelest "Päike" | "heelium" | |
| Raud | Fe rrum | Alates Lat. "mõõk" | "raud" | |
| Kuldne | Au rumm | Alates Lat. "põlemine" | "aurum" | |
| Jood | I odum | Kreeka keelest " violetne" | "jood" | |
| Kaalium | K alium | Araabia keelest "leelis" | "kaalium" | |
| Kaltsium | Ca ltsium | Alates Lat. "lubjakivi" | "kaltsium" | |
| Hapnik | O xygenium | Kreeka keelest "hapet tekitav" | "O" | |
| Räni | Si licium | Alates Lat. "tulekivi" | "räniium" | |
| Krüpton | Kr ypton | Kreeka keelest "peidetud" | "krüpton" | |
| Magneesium | M a g neesium | Nime järgi Magneesia poolsaar | "magneesium" | |
| Mangaan | M a n ganum | Kreeka keelest "puhastamine" | "mangaan" | |
| Vask | Cu prum | Kreeka keelest nimi O. Küpros | "kupp" | |
| Naatrium | Na trium | araabia keelest "pesuvahend" | "naatrium" | |
| Neoon | Ne peal | Kreeka keelest "uus" | "neoon" | |
| Nikkel | Ni ccolum | Temalt. "Püha Nikolai Vask" | "nikkel" | |
| elavhõbe | H ydrar g irum | Lat. "vedel hõbe" | "hüdrargyrum" | |
| Plii | P lum b um | Alates Lat. plii ja tina sulami nimetused. | "plumbum" | |
| Väävel | S väävel | Sanskriti keelest "põlev pulber" | "es" | |
| Hõbedane | A r g entum | Kreeka keelest " valgus" | "argentum" | |
| Süsinik | C arboneum | Alates Lat. "kivisüsi" | "tse" | |
| Fosfor | P fosforit | Kreeka keelest "valguse tooja" | "peh" | |
| Fluor | F luorum | Alates Lat. tegusõna "voolama" | "fluor" | |
| Kloor | Cl orum | Kreeka keelest "rohekas" | "kloor" | |
| Kroom | C h r omium | Kreeka keelest "värv" | "kroom" | |
| Tseesium | C ae s ium | Alates Lat. "taevasinine" | "tseesium" | |
| Tsink | Z i n cum | Temalt. "tina" | "tsink" | |
2.3. Keemilised valemid
Kasutatakse keemiliste ainete tähistamiseks keemilised valemid.
Molekulaarsete ainete puhul võib keemiline valem tähistada selle aine ühte molekuli.
Teave aine kohta võib olla erinev, seega on see erinev keemiliste valemite tüübid.
Sõltuvalt teabe täielikkusest jagatakse keemilised valemid nelja põhitüüpi: algloomad,
molekulaarne, struktuurne Ja ruumiline.
Lihtsaimas valemis olevatel alaindeksitel pole ühist jagajat.
Indeksit "1" valemites ei kasutata.
Näited kõige lihtsamatest valemitest: vesi - H 2 O, hapnik - O, väävel - S, fosforoksiid - P 2 O 5, butaan - C 2 H 5, fosforhape - H 3 PO 4, naatriumkloriid (lauasool) - NaCl.
Lihtsaim vee valem (H 2 O) näitab, et vee koostis sisaldab elementi vesinik(H) ja element hapnikku(O) ja vee mis tahes osas (osa on osa millestki, mida saab jagada oma omadusi kaotamata.) on vesinikuaatomite arv kaks korda suurem kui hapnikuaatomite arv.
Osakeste arv, kaasa arvatud aatomite arv, mida tähistatakse ladina tähega N. Tähistab vesinikuaatomite arvu - N H ja hapnikuaatomite arv on N Oh, me võime seda kirjutada
Või N H: N O=2:1.
Fosforhappe (H 3 PO 4) lihtsaim valem näitab, et fosforhape sisaldab aatomeid vesinik, aatomid fosforit ja aatomid hapnikku, ja nende elementide aatomite arvu suhe fosforhappe mis tahes osas on 3:1:4, see tähendab
NH: N P: N O = 3:1:4.

Lihtsaima valemi saab koostada iga üksiku keemilise aine jaoks ja molekulaarse aine jaoks lisaks saab selle koostada molekulaarne valem.
Molekulaarvalemite näited: vesi - H 2 O, hapnik - O 2, väävel - S 8, fosforoksiid - P 4 O 10, butaan - C 4 H 10, fosforhape - H 3 PO 4.
Mittemolekulaarsetel ainetel pole molekulaarseid valemeid.
Liht- ja molekulaarvalemites elementide sümbolite kirjutamise järjekord määratakse keemilise keele reeglitega, millega tutvute keemiat õppides. Nende valemitega edastatavat teavet sümbolite jada ei mõjuta.
Ainete struktuuri kajastavatest märkidest kasutame praegu vaid valents insult("kriips"). See märk näitab olemasolu aatomite vahel nn kovalentne side(mis tüüpi ühendus see on ja millised on selle omadused, saate varsti teada).

Veemolekulis on hapnikuaatom ühendatud lihtsate (üksik)sidemete kaudu kahe vesinikuaatomiga, kuid vesinikuaatomid ei ole omavahel seotud. Just seda näitab selgelt vee struktuurivalem. ![]()
Teine näide: väävlimolekul S8. Selles molekulis moodustavad 8 väävliaatomit kaheksaliikmelise ringi, milles iga väävliaatom on ühendatud kahe teise aatomiga lihtsidemetega. Võrrelge väävli struktuurivalemit selle molekuli kolmemõõtmelise mudeliga, mis on näidatud joonisel fig. 3. Pange tähele, et väävli struktuurivalem ei anna edasi selle molekuli kuju, vaid näitab ainult kovalentsete sidemetega aatomite ühendamise järjestust.

Fosforhappe struktuurivalem näitab, et selle aine molekulis on üks neljast hapnikuaatomist topeltsidemega seotud ainult fosfori aatomiga ja fosfori aatom omakorda veel kolme hapnikuaatomiga üksiksidemetega. . Kõik need kolm hapnikuaatomit on samuti lihtsa sidemega ühendatud ühega kolmest molekulis olevast vesinikuaatomist.
Võrrelge järgmist metaani molekuli kolmemõõtmelist mudelit selle ruumilise, struktuurse ja molekulaarse valemiga:
|
|
|
Metaani ruumivalemis näitavad kiilukujulised valentsilöögid justkui perspektiivis, milline vesinikuaatomitest on “meile lähemal” ja milline “meist kaugemal”.
Mõnikord näitab ruumivalem sideme pikkusi ja sidemete vahelisi nurki molekulis, nagu on näidatud veemolekuli näites.

Mittemolekulaarsed ained ei sisalda molekule. Keemiliste arvutuste hõlbustamiseks mittemolekulaarses aines kasutatakse nn valemiühik.
Mõnede ainete valemiühikute koostise näited: 1) ränidioksiid (kvartsliiv, kvarts) SiO 2 – valemiühik koosneb ühest räni- ja kahest hapnikuaatomist; 2) naatriumkloriid (lauasool) NaCl – valemiühik koosneb ühest naatriumi- ja ühest klooriaatomist; 3) raud Fe - valemiühik koosneb ühest raua aatomist.Nagu molekul, on ka valemiühik aine väikseim osa, mis säilitab oma keemilised omadused.
Tabel 4
Teave, mida edastatakse erinevat tüüpi valemitega
Valemi tüüp |
Valemiga edastatud teave. |
|
| Kõige lihtsam Molekulaarne Struktuurne Ruumiline |
|
|
Vaatleme nüüd näidete abil, millist teavet eri tüüpi valemid meile annavad.
1. Aine: äädikhape. Lihtsaim valem on CH 2 O, molekulvalem on C 2 H 4 O 2, struktuurvalem

Lihtsaim valemütleb meile seda
1) äädikhape sisaldab süsinikku, vesinikku ja hapnikku;
2) selles aines on süsinikuaatomite arv seotud vesinikuaatomite arvu ja hapnikuaatomite arvuga 1:2:1, see tähendab N H: N C: N O = 1:2:1.
Molekulaarvalem lisab selle
3) äädikhappe molekulis on 2 süsinikuaatomit, 4 vesinikuaatomit ja 2 hapnikuaatomit.
Struktuurivalem lisab selle
4, 5) molekulis on kaks süsinikuaatomit omavahel ühendatud lihtsidemega; üks neist on lisaks ühendatud kolme vesinikuaatomiga, millest igaüks on üksiksidemega, ja teine kahe hapnikuaatomiga, millest üks on kaksikside ja teine üksiksidemega; viimane hapnikuaatom on endiselt ühendatud lihtsidemega neljanda vesinikuaatomiga.
2. Aine: naatriumkloriid.
Lihtsaim valem on NaCl.
1) Naatriumkloriid sisaldab naatriumi ja kloori.
2) Selles aines on naatriumi aatomite arv võrdne kloori aatomite arvuga.
3. Aine: raud.
Lihtsaim valem on Fe.
1) See aine sisaldab ainult rauda, see tähendab, et see on lihtne aine.
4. Aine: trimetafosforhape . Lihtsaim valem on HPO 3, molekulvalem on H 3 P 3 O 9, struktuurvalem
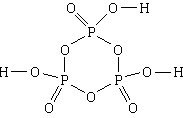
1) Trimetafosforhape sisaldab vesinikku, fosforit ja hapnikku.
2) N H: N P: N O = 1:1:3.
3) Molekul koosneb kolmest vesinikuaatomist, kolmest fosfori aatomist ja üheksast hapnikuaatomist.
4, 5) Kolm fosfori- ja kolm hapnikuaatomit vaheldumisi moodustavad kuueliikmelise tsükli. Kõik tsükli ühendused on lihtsad. Iga fosfori aatom on lisaks ühendatud veel kahe hapnikuaatomiga, millest üks on kaksikside ja teine üksiksidemega. Kõik kolm hapnikuaatomit, mis on ühendatud lihtsate sidemetega fosfori aatomitega, on samuti ühendatud lihtsa sidemega vesinikuaatomiga.
| Fosforhape - H3PO4(teine nimi on ortofosforhape) on läbipaistev, värvitu, molekulaarse struktuuriga kristalne aine, mis sulab temperatuuril 42 o C. See aine lahustub väga hästi vees ja imab isegi õhust veeauru (hügroskoopne). Fosforhapet toodetakse suurtes kogustes ja seda kasutatakse eelkõige fosfaatväetiste tootmisel, aga ka keemiatööstuses, tikkude valmistamisel ja isegi ehituses. Lisaks kasutatakse fosforhapet tsemendi valmistamisel hambaravitehnoloogias ja see sisaldub paljudes ravimites. See hape on üsna odav, seetõttu lisatakse mõnes riigis, näiteks USA-s, värskendavatele jookidele kalli sidrunhappe asemel väga puhast, veega tugevalt lahjendatud fosforhapet. |
| Metaan – CH 4. Kui teil on kodus gaasipliit, siis kohtate seda ainet iga päev: teie pliidi põletites põlev maagaas koosneb 95% metaanist. Metaan on värvitu ja lõhnatu gaas, mille keemistemperatuur on –161 o C. Õhuga segunedes on see plahvatusohtlik, millega on seletatav söekaevandustes (teine metaani nimi on firedamp) mõnikord esinevad plahvatused ja tulekahjud. Metaani kolmas nimetus – rabagaas – tuleneb sellest, et selle konkreetse gaasi mullid tõusevad soode põhjast üles, kus see tekib teatud bakterite tegevuse tulemusena. Tööstuses kasutatakse metaani kütusena ja toorainena muude ainete tootmiseks.Metaan on kõige lihtsam süsivesinik. Sellesse ainete klassi kuuluvad ka etaan (C 2 H 6), propaan (C 3 H 8), etüleen (C 2 H 4), atsetüleen (C 2 H 2) ja paljud teised ained. |
Tabel 5.Mõnede ainete erinevat tüüpi valemite näited-
Sarnased artiklid
-
Jove - kena mees ja World Of Tanks peaprodutsent Mihhail "Storm" Zyvets
Konstantin “Jove” Ladanin, sündinud 12. juunil 1986. Jove on kultusmängu World Of Tanks mõjukaim mängija. See sai populaarseks pärast iganädalasi väljalaseid koos mängude läbimisega. Jov peab ka oma isiklikku blogi, kus...
-
Polkatants lasteaia liikumises
Proovime koos selgeks õppida mõned põhilised polka liigutused, mida kasutatakse paljudes seltskonna- ja rahvatantsudes. See tants on sageli kaasatud laste ballisaalide ja koreograafiliste rühmade repertuaari.Astu hüppega Kõige...
-
Vladislav Listjevi mõrva juhtum
0 4. aprill 2013, 14:45 Täna ilmus veebis intervjuu, mille Konstantin Ernst andis Jevgeni Levkovitšile arvatavasti ajakirja Rolling Stones jaoks, milles Channel One peadirektor nimetas Vladislavi mõrva tellija...
-
"Kes on Oleg Feoktistov"
SEB FSB (finantssektori vastuluure) K-osakonna juhataja Ivan Tkatšov on eriti salajane inimene, kannab vormiriietust harva, seni pole tema fotosid Internetis olnud ja tema sugulased ei teadnud, mida. ta teeb. Kindralmajor...
-
Rutskoy Aleksander Vladimirovitš - elulugu
POLIITILINE PORTREE Venemaa perestroika rahutu õhkkond tõi esile palju värvikaid tegelasi, kellest said tema poliitilisel areenil silmapaistvad tegelased. Üks hämmastavamaid tõuse (isegi seiklusliku karjääri taustal...
-
Metroloogia test Metroloogia testid mõõtmiste klassifikatsioon
TESTIÜLESANDED 1. Metroloogia on... a) füüsikaliste suuruste ühikute suuruste ülekandmise teooria; b) algmõõtevahendite (standardite) teooria; c) mõõtmiste teadus, nende ühtsuse tagamise meetodid ja vahendid ning viisid, kuidas saavutada...


